Are you a journalist? Please sign up here for our press releases
Subscribe to our monthly newsletter:
פציעה או תהליכי הזדקנות עלולים להוביל להיווצרות רקמת צלקת (פיברוזיס) באיברים פנימיים כמו לב, ריאה, כליות או כבד, אבל בניגוד לתפיסה רווחת בעולם הרפואה לא כל הצלקות זהות – זו המסקנה העולה ממחקר חדש של מדעני מכון ויצמן למדע. הממצאים המתפרסמים היום בכתב-העת המדעי Cell Systems חושפים כי במחלות לב שונות נוצרים שני סוגים שונים של רקמת צלקת – "פיברוזיס חם" ו"פיברוזיס קר" – וכי כל אחד מהם מחייב גישה טיפולית שונה. התגלית עשויה להוביל לטיפולים קרדיולוגיים חדשניים ואף סוללת את הדרך למחקרים על פיברוזיס באיברים אחרים.
המחקר החל כשיתוף פעולה בין שכנים במכון ויצמן. פרופ' אלדד צחור, שמחקריו מתמקדים בלב ובמחלותיו, שמע על מודל מתמטי שנוצר במעבדה הסמוכה שבראשה עומד פרופ' אורי אלון. המודל של פרופ' אלון הציע לסווג רקמת צלקת באיברים שונים על סמך נוכחותם של שני סוגי תאים בלבד: פיברובלסטים – תאים יצרני קולגן המספקים לרקמות תמיכה ומבנה – ותאים של המערכת החיסונית הנקראים מקרופאגים.

"בהתחלה זה היה נשמע לי פשטני מדי – הרי כולנו יודעים עד כמה מורכבות המערכות הביולוגיות. אבל הרעיון סיקרן אותי, ואולי זה היה רק תירוץ לשתף פעולה עם אורי", מתוודה פרופ' צחור. "אז הצעתי לו שננסה ליישם את המודל על מחלות לב".
בלב נוצרת רקמת צלקת כשתאי שריר הלב נפגעים, למשל בעקבות התקף לב. בדומה לטלאי המתקן חור בבגד, צלקת המחליפה תאים פגועים מאפשרת ללב להמשיך לתפקד כמשאבת הדם של הגוף. עם זאת, רקמה זו אינה מתכווצת ביעילות, והיא אף עלולה להתפשט ולהוביל בסופו של דבר לפגיעה בתפקוד הלב. מכיוון שאין כיום טיפול יעיל לצלקות לב, הרפואה מנסה למנוע את היווצרותן או לצמצם את היקפן.
"רקמת צלקת בלב עשויה להיראות לכאורה פשוטה יחסית, אך תהליך היווצרותה הינו מורכב ביותר ומעורבים בו הרבה מאוד סוגי תאים ומולקולות", אומר שובל מיארה, תלמיד דוקטורט משותף של הפרופסורים צחור ואלון, שהוביל את המחקר יחד עם ד"ר מירי אדלר מהאוניברסיטה העברית בירושלים, סטודנטית לשעבר של פרופ' אלון. "כדי להתמודד עם המורכבות הביולוגית ולחתור ללב העניין, ניגשנו לאתגר כמו אמן המנסה לזקק את המהות מתוך העולם הרועש שסביבנו – כמו השור המפורסם של פיקאסו שנישאר שור גם כשהוא משורטט בכמה קווים בודדים".
""בספרי הרפואה, תמונות מיקרוסקופיה של צלקות בשריר הלב נראות אותו הדבר. אנחנו הראינו שמדובר בשתי מחלות לב שונות, ולכן יש גם לטפל בהן ולפתח עבורן תרופות באופן שונה"
ה"שור" ששירטטו החוקרים בעזרת המודל המתמטי של פרופ' אלון נגח בסופו של דבר במוסכמה הרפואית הרואה את כל הצלקות בלב באופן שווה. המודל חזה שני מנגנונים שונים להיווצרות צלקות בלב. האחד, מנגנון שבו מתפתחת רקמת הצלקת כתוצאה מקשרי הגומלין והתקשורת בין מיופיברובלסטים – פיברובלסטים בעלי יכולת התכווצות המאפיינים את רקמת הצלקת בלב – ובין מקרופאגים של המערכת החיסונית, והאחר, מנגנון במעגל סגור שבו המיופיברובלסטים מסתדרים בעצמם ללא שותפים ומעודדים את התפתחות הצלקת באמצעות מולקולות שהם עצמם מפרישים. מכיוון שמעורבות של מערכת החיסון מזוהה לרוב עם חום ודלקת, המנגנון הראשון כונה "פיברוזיס חם" – בעוד המנגנון האחר זכה לשם "פיברוזיס קר".
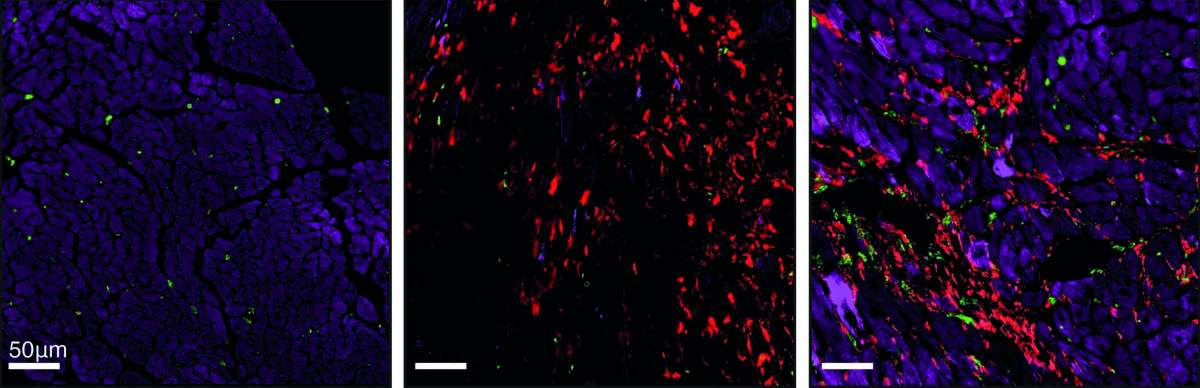
כאשר מיארה והצוות העמידו את המודל במבחן המציאות – תחילה בתרביות תאים ובעכברים – הם קיבלו חיזוק לתחזיותיו המפתיעות. החוקרים ראו כי בעוד אי ספיקת לב כרונית של הלב מובילה לפיברוזיס חם עם נוכחות רבה של מקרופאגים, פגיעה אקוטית, כמו התקף לב, מובילה לפיברוזיס קר. אמנם מיד לאחר התקף הלב יש נוכחות של תאי המערכת החיסונית, אך תוך כמה שבועות כמעט שלא נותרים מקרופאגים ברקמת הצלקת. בשלב הבא, שוחזרו ממצאים אלה גם בדגימות אנושיות של רקמת לב.
אבל החוקרים לא עצרו בשלב אישוש המודל – הם הצליחו לזהות מולקולת מפתח שמשפיעה על התפתחות הצלקת בפיברוזיס קר: חלבון בשם TIMP-1 שהיה מוכר בהקשרים אחרים, אך התגלה כאן לראשונה כגורם גדילה המקדם את חלוקת המיופיברובלסטים ואת יצירת רקמת הצלקת בלב. כאשר המדענים חסמו את TIMP-1 בעכברים לאחר התקף לב, רקמת הצלקת שנוצרה בשריר הלב שלהם הייתה קטנה יותר בהשוואה לעכברים שלא טופלו.
"הראינו ש-TIMP-1 הוא יעד פוטנציאלי לתרופות עתידיות נגד פיברוזיס, אבל ברור שהוא לא היחיד", אומר מיארה. "מחקר המשך יכול לחשוף יעדים נוספים, ולהראות במי מהם ניתן להתמקד בצורה היעילה ביותר כדי למנוע או למזער נזק לשריר הלב לאחר התקף לב".

"בספרי הרפואה, תמונות מיקרוסקופיה של פתולוגיות בשריר הלב נראות אותו הדבר – רואים בהן בדרך כלל את סיבי הקולגן המרכיבים את רקמת הצלקת, אך אנחנו הראינו שפיברוזיס חם ופיברוזיס קר הם תולדה של מנגנונים ביולוגיים שונים. כלומר, מדובר בשתי מחלות לב שונות, ולכן יש גם לטפל בהן ולפתח עבורן תרופות באופן שונה". מסכם פרופ' צחור. "שיתוף הפעולה פתח את ליבי לביולוגיה המרתקת של הלב", אומר פרופ' אלון. "מחקרים עתידיים יוכלו ליישם את הגישה שלנו, המשלבת בין מודלים מתמטיים, ביולוגיה בסיסית וצרכים רפואיים, גם באיברים אחרים ולבדוק אם החלוקה לפיברוזיס חם וקר חלה על צלקות של רקמות אחרות – בריאה, בכליות או בכבד – ואפילו בצלקות המתפתחות בעקבות סרטן או שבץ מוחי".
במחקר השתתפו גם ד"ר כפיר-ברוך אומנסקי, ילין דיוינסקי, יעקב אלקהל, ד"ר דוד קין, ד"ר דריה לנדנגולץ, ד"ר חנה בואנו-לוי, ד"ר אלכסנדר גנזלינח, דניאל קמחי, ד"ר אברהם שקד, ד"ר לינגלינג זאנג, זכריה פטרובר, ד"ר רחל סריג וד"ר אבי מאיו מהמחלקה לביולוגיה מולקולרית של התא של המכון; דניאל האוסלר ופרופ' אכים קרוגר מהאוניברסיטה הטכנית של מינכן; ד"ר אלעד בשט, ד"ר ג'ינגקוי וואנג ופרופ' אלי טנאקה מהביוסנטר של וינה; ד"ר ריקארדו רמירז פלורס ופרופ' חוליו סז-רודריגז מאוניברסיטת היידלברג; ד"ר עפרה גולני מהמחלקה לתשתיות מחקר מדעי החיים של המכון; ד"ר טלי שליט, מיכאל גרשוביץ ואביתר ויצמן מהמרכז הישראלי הלאומי לרפואה מותאמת אישית ע"ש ננסי וסטיבן גרנד; ד"ר אנדראה בר, ד"ר טטיאנה דורן, פרופ' אלסנדרה מורטי ופרופ' כריסטיאן קופט מהמרכז הגרמני לחקר הלב וכלי הדם (DZHK) ופרופ' רוסלן מדג'יטוב מבית הספר לרפואה של אוניברסיטת ייל.
בחדר השמאלי של הלב האנושי יש כ-4 מיליארד תאי שריר לב. ההערכה היא שכ-25 אחוז מהם, כלומר 1 מיליארד תאים, מתים במהלך התקף לב.