Are you a journalist? Please sign up here for our press releases
Subscribe to our monthly newsletter:
מדעני המכון גילו, שהפעילות המחזורית של חיידקי המעיים משפיעה לא רק על סביבתם הקרובה, אלא גם על איברים בגוף המרוחקים מהם, כמו הכבד. השפעה זו מתוּוכת באמצעות הפרשת מטבוליטים, שהן מולקולות קטנות המעורבות בחילוף חומרים, וכן השריית שינויים אפיגנטיים, ובאמצעותם יכולים החיידקים להשפיע על קצב פירוק תרופות בכבד.

חיידקי המעיים משפיעים על הפיסיולוגיה שלנו ועל תיפקודם של איברים שונים בגופנו. מסקנה מרחיקת לכת זו עולה ממחקר של מדעני מכון ויצמן למדע שפורסם באחרונה בכתב-העת המדעי CELL. במחקר קודם של חברי קבוצות המחקר של ד"ר ערן אלינב מהמחלקה לאימונולוגיה ושל פרופ' ערן סגל מהמחלקה למתמטיקה שימושית ומדעי המחשב, עלה שהשעון הביולוגי של המארח משפיע על זמני האכילה של עכברים ובני אדם, ובאמצעותם על השעון הביולוגי של חיידקי המעיים, שאוכלוסייתם ותיפקודם משתנים באופן מחזורי במשך שעות היום. "במחקר הנוכחי", אומר ד"ר אלינב, "שאלנו את השאלה ההפוכה: כיצד משפיעה הפעילות המחזורית של חיידקי המעיים על הפיסיולוגיה של המארח, ומה הם המנגנונים שבאמצעותם מופעלת ההשפעה הזאת".
בשלב הראשון במחקרם שיבשו המדענים את פעילותם המחזורית של חיידקי המעי באמצעות מתן אנטיביוטיקה, וגילו שהפרעה זו משפיעה ישירות על הביטוי המחזורי של הגנים שבמעי העכברים. "מצאנו", אומר פרופ' סגל, "שבקבוצה אחת של גנים במעי, המחזוריות נותרה כשהייתה, על אף ההפרעה לחיידקים; בקבוצת גנים אחרת פסקה לחלוטין ההתנהגות המחזורית; ובקבוצת גנים שלישית החלה פעילות מחזורית שלא התחוללה לפני כן".
תלמידי המחקר כריסטוף טהייס ומעיין לוי, ממעבדתו של ד"ר אלינב, הובילו את המחקר. הם שיתפו פעולה עם תלמיד המחקר טל כורם ממעבדתו של פרופ' סגל, ומצאו שהמנגנון המאפשר את השפעת החיידקים על הגנים במעי המארח הוא השראה אפיגנטית. "כלומר", מסביר ד"ר אלינב, "החיידקים גורמים לאזורים מסוימים בדי-אן-אי של תאי המארח להיות גלויים, או נסתרים, למנגנונים שמבטאים אותם. בדרך זו הם משפיעים על 'השעון הביולוגי' באותם גנים".
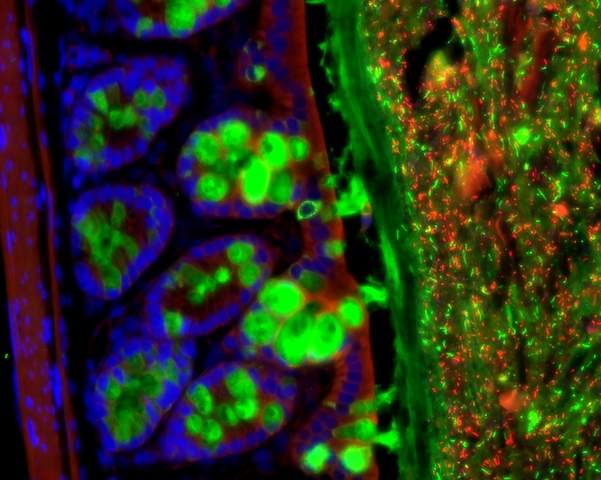
בשלב הבא בדקו המדעים אם בכוחם של חיידקי המעיים להשפיע לא רק על סביבתם הקרובה, אלא גם על איברים בגוף הממוקמים במרחק רב מהם, כמו הכבד. מחקר זה בוצע בעכברים חסרי חיידקי מעיים (Germ-free), או בכאלה שטופלו באנטיביוטיקה המשבשת את הפעילות המחזורית של חיידקי המעי שלהם. כך נמצא, שביטוי הגנים המחזורי בכבד הושפע מנוכחות החיידקים במעיים בצורה דומה לזו של ביטוי הגנים המחזורי במעיים: הפעילות המחזורית של חלק מהגנים של הכבד לא הושפעה מהחיידקים, ואילו מאות גנים אחרים איבדו את פעילותם המחזורית, או שהחלה אצלם התנהגות מחזורית בעקבות השריית שינויים בחיידקי המעי.
השפעה מפתיעה זו של החיידקים על פעילות גנטית המתרחשת הרחק ממקום הגידול שלהם, גילו המדענים, מתוּוכת באמצעות הפרשת "מטבוליטים" (מולקולות קטנות הממלאות תפקיד בחילוף החומרים בגוף). המטבוליטים, שגם להם פעילות מחזורית המתואמת עם זו של החיידקים, מגיעים לאיברי הגוף ממערכת העיכול דרך זרם הדם. פגיעה בפעילות המחזורית של החיידקים במעי הביאה לפגיעה בהתנהגות המחזורית של המטבוליטים בדם, ולשינויים בפעילות המחזורית של הכבד. "באמצעות השפעה על הפרשה ושינוי מולקולות קטנות במעי, יכולים חיידקי המעי להתוות שינויים גנטיים באיבר מרוחק כמו הכבד, שבעצמו הוא חסר חיידקים", מסבירים המדענים.
האם להשפעות המחזוריות של החיידקים על פעילותו המחזורית של הכבד יש חשיבות רפואית? במטרה לענות על שאלה זו התרכזו המדענים בפעילות כבד מטבולית חיונית ומרכזית – פירוק תרופות. ידוע כי מנת יתר של פָּרָצֶטָמוֹל ("אקמול", למשל, הוא שם מסחרי של תרופה זו) – תרופה נפוצה המפורקת ביעילות בכבד – משבשת את מנגנוני הפירוק בכבד, וגורמת "רַעֶלֶת אקמול" ונזק לכבד. בניסויים בעכברים התברר שקצב פירוק התרופה, ולכן גם רמת הרעילות שנוצרת עקב מתן-יתר שלה, שונה בתכלית כאשר התרופה ניתנת בשעות היום, בהשוואה לתרופה שניתנה בשעות הלילה. אך הפרעה לפעילות המחזורית של חיידקי המעי בעכברים – כך התגלה – מביאה לרעילות פרצטמול נמוכה, שרמתה קבועה לאורך כל שעות היום. מכאן ניתן להסיק, שהתערבות בפעילותם המחזורית של חיידקי המעיים עשויה להשפיע על האופן שבו תרופה מסוימת מפורקת בכבד, ועל נטייתה להיות רעילה. "ממצאים אלה", מסביר פרופ' סגל, "יכולים אולי להסביר מנגנונים של תופעות לוואי שעד היום לא ידענו כיצד להסבירן; למשל, הופעתה של נטייה להשמנה אצל מבוגרים שנטלו אנטיביוטיקה בילדותם".
מוסיף ד"ר אלינב: ״כעת אנחנו מבינים את 'ריקוד הטנגו' ההדוק שבין הפעילות המחזורית של חיידקי המעי לבין פעילות השעון הביולוגי בגופנו, ובזכות זאת אולי יתאפשרו התערבויות חיידקיות אשר ישפיעו על פעילויות גופניות חשובות המתרחשות הרחק ממקום מושבם של החיידקים, כמו תגובה לתרופות ופירוקן, וכן מניעת הרעלות עקב נטילתן״.
עוד השתתפו במחקר: ד"ר מירב פבסנר-פישר, ד"ר מלי בכש, ד"ר חגית שפירא, לנקה דונלובה, יבגני טטרובסקי, טימור טוגאנבאב, ד"ר שרה פדריצ'י, וד"ר ניב זמורה ממעבדתו של ד"ר אלינב במחלקה לאימונולוגיה; דוד זאבי ממעבדתו של פרופ' סגל במחלקה למדעי המחשב ומתמטיקה שימושית; פרופ' עידו עמית וחוקרי מעבדתו, ד"ר דייגו חייטין, איל דוד, דבורה וינטר, מיטל גורי-בן ארי; ד"ר ילנה קרטבלישוילי מהמחלקה לתשתיות למחקר כימי; ד"ר אלכסנדר ברנדיס מהיחידה לתשתיות מחקר מדעי החיים; פרופ' אלון הרמלין מהמחלקה למשאבים וטרינריים; פרופ' אורן שיבולת ופרופ' זמיר הלפרן מהפקולטה לרפואה ע"ש סאקלר באוניברסיטת תל-אביב והמרכז הרפואי תל אביב על-שם סוראסקי; ופרופ' קניה הודנה ממרכז RIKEN לרפואה אינטגרטיבית, יפן.
רעילות בכבד עקב נטילת פָּרָצֶטָמוֹל ("אקמול") גורמת ל-25% ממקרי כשל כבדי בילדים. #מספרי_מדע |